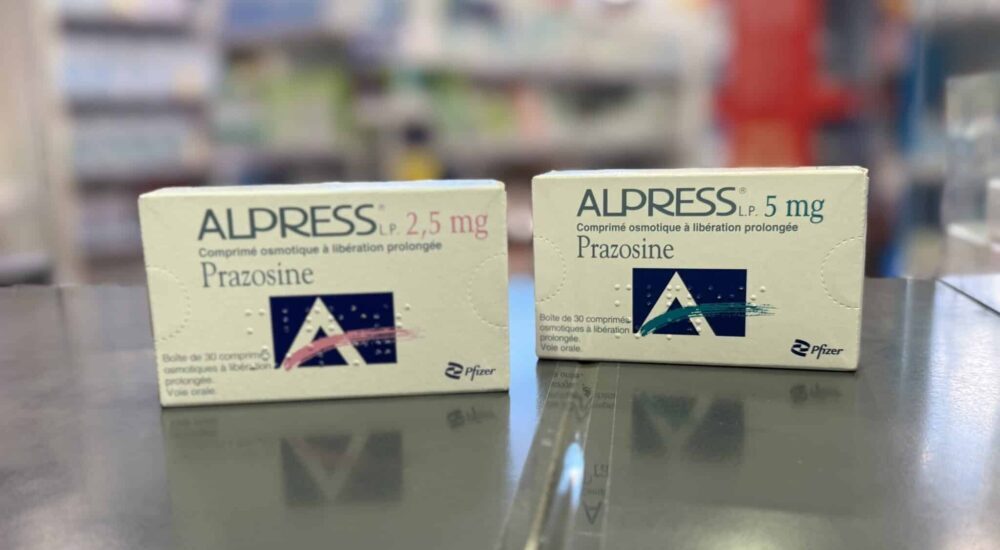
ALPRESS L.P. tire sa révérence : une transition thérapeutique à anticiper
À compter du 1er septembre 2025, les spécialités ALPRESS L.P.® 2,5 mg et 5 mg (prazosine LP) seront retirées du marché. Une réévaluation des traitements s’impose.
Un retrait progressif, mais définitif
Pfizer met un terme à la commercialisation d’ALPRESS L.P.® (chlorhydrate de prazosine) à libération prolongée, dosée à 2,5 mg et 5 mg.
L’arrêt interviendra le 1er septembre 2025, mais les stocks existants pourront être écoulés jusqu’à leur péremption — mars ou juin 2027 selon les présentations.
Une annonce qui impose d’anticiper la transition thérapeutique des patients encore stabilisés sous cette molécule historique.
Une molécule emblématique, aujourd’hui marginale
Alpha-bloquant de première génération, la prazosine a longtemps occupé une place dans le traitement de l’hypertension artérielle (HTA), notamment chez les patients en polythérapie ou résistants aux traitements de première ligne.
Mais les recommandations actuelles (HAS, ESC, ESH) ont progressivement relegué cette molécule derrière les IEC, ARA2, inhibiteurs calciques et diurétiques thiazidiques, mieux documentés sur la mortalité cardiovasculaire.
Elle conserve toutefois un intérêt ciblé dans certaines situations :
-
hypertrophie bénigne de la prostate,
-
syndrome de Raynaud,
-
HTA secondaire.
La disparition de sa forme à libération prolongée, souvent mieux tolérée et favorisant l’adhésion, risque donc de déséquilibrer certains patients chroniques bien stabilisés depuis plusieurs années.
Quelles options de relais ?
Les relais pharmacologiques se dessinent selon deux axes : le maintien d’un alpha-bloquant ou la substitution inter-classes.
1. Relais de même classe
-
Doxazosine (Zoxan®, Doxatens®…) : autre alpha-bloquant, disponible en comprimés LP, avec une cinétique et une posologie proches.
-
Urapidil (Eupressyl®) : également indiqué dans l’HTA et disponible en formes orales pour un relais progressif.
2. Relais d’autres classes antihypertensives
Selon le profil cardiovasculaire, la tolérance et le risque iatrogénique, d’autres options restent les piliers de la stratégie :
-
IEC : ramipril, périndopril…
-
ARA2 : losartan, valsartan…
-
Inhibiteurs calciques : amlodipine, félodipine…
-
Diurétiques thiazidiques : indapamide, hydrochlorothiazide…
Un relais mal conduit expose à un rebond tensionnel ; un suivi clinique et tensionnel rapproché est donc essentiel, notamment les premières semaines.
Le rôle pivot de l’officine
Nous sommes en première ligne pour repérer, informer et sécuriser cette transition.
Chaque renouvellement d’ALPRESS L.P.® doit être l’occasion :
-
d’informer le patient du retrait progressif,
-
d’anticiper la substitution avant la rupture définitive,
-
d’orienter vers le médecin pour réévaluation du schéma thérapeutique.
Points clés de vigilance officinale
-
Identifier tout patient encore sous prazosine LP.
-
Anticiper la rupture et proposer un relais (doxazosine LP ou autre classe).
-
Surveiller la survenue de céphalées, vertiges, hypotensions orthostatiques lors du changement de molécule.
-
Encourager un autocontrôle tensionnel à domicile (tensiomètre validé, carnet de suivi).
-
Rassurer : des alternatives efficaces et bien tolérées existent.
Maintenir la continuité thérapeutique
La consultation du dossier pharmaceutique, couplée à une concertation interprofessionnelle (médecin traitant, cardiologue, infirmier), permet de sécuriser la transition et de prévenir toute décompensation tensionnelle.
Plus que jamais, l’accompagnement officinal, le suivi tensionnel régulier et la pédagogie au comptoir constituent les garants d’une prise en charge continue et sécurisée.
 Se connecter
Se connecter